|
La legge di Boyle-Mariotte
La legge di Boyle-Mariotte afferma:
Il volume di una quantità di gas perfetto V a
temperatura costante, è inversamente proporzionale alla pressione assoluta p,
ossia il prodotto della pressione assoluta per il volume è costante per una
determinata quantità di gas.
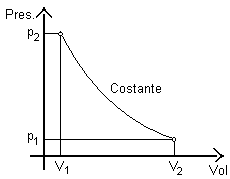

quindi p1 ·
V1 = p2
· V2 = p3 · V3
= a una costante
All'incrementare della pressione esercitata il volume dell'aria si riduce
proporzionalmente questo implica che la pressione esercitata moltiplicata per il
volume del gas è uguale ad una costante.
Prima legge di Guy-Lussac
La prima legge di Guy-Lussac afferma:
Il volume dell'aria, a pressione costante,
varia in modo proporzionale al variare della temperatura, misurata in valori
assoluti Kelvin.
L'aria a pressione costante se si riscalda di
1° Kelvin si espande di circa 1/273 del suo volume.
Sia
V1= volume alla temperatura 1
V2 = volume alla temperatura 2
T1 = temperatura 1
T2 = temperatura 2
V2
= V1 + (V1/273)
· (T2
- T1)
Seconda legge di Guy-Lussac
La seconda legge di Guy-Lussac afferma:
Dato un volume d'aria costante, la pressione
varia in modo proporzionale al variare della temperatura, misurata in valori
assoluti Kelvin.
Espressione delle tre leggi
La due Leggi di Guy-Lussac e quella di Boyle-Mariotte possono
essere espresse come:
p · v = m
· R
· T
dove
- p è la pressione assoluta in Pa
- v è il volume specifico (volume all'unità di massa)
in m³
- m massa del gas in kg
- T è la temperatura in gradi Kelvin
- R è la costante del gas, che per
l'aria assume il valore di 287 [J/(Kg K)].
Questa equazione e le precedenti sono
valide solo per i gas perfetti. Danno comunque dei buoni
risultati anche con i gas reali puri come azoto, ossigeno,
idrogeno e con miscele di gas come nel caso dell'aria. |